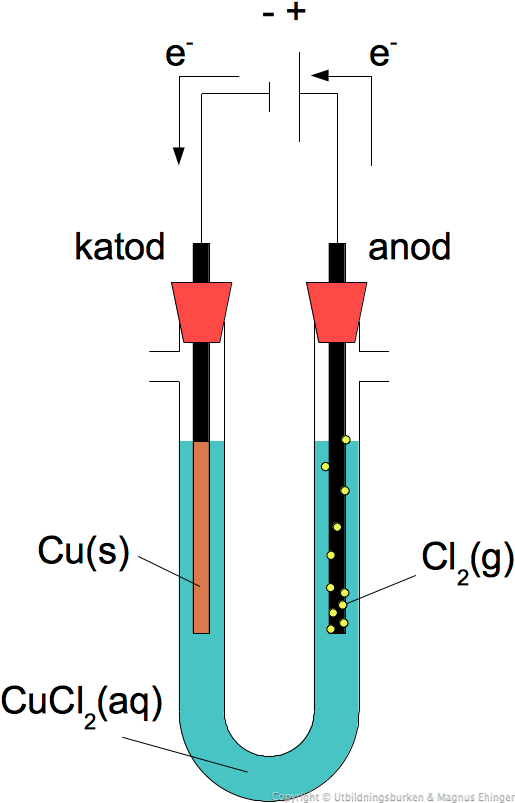
Elektrolys
Vad är en elektrolys?
Med hjälp av elektrisk ström kan man driva reaktioner. Utnyttjad elektrisk energi för att få till stånd-kemiska reaktioner kallas elektrolys. En elektrolys är alltså när man använder elektrisk ström för att få till en kemisk reaktion.
Joner istället för fria elektroner som driver ström
Minuspolen på en strömkälla (ett batteri) pumpar ut elektroner och pluspolen suger till sig elektroner. När det går ström som går genom metaller och kol(grafit) är det fria elektroner som rör sig mellan atomerna.
Men vattenlösningar som leder ström innehåller inga fria elektroner utan här är det joner som står för strömtransporter.
En jon är ett grundämne som har fler eller färre elektroner än protoner i kärnan. Detta gör att jonen är laddad. Det finns alltså negativa joner och positiva joner. Positiva och negativa joner brukar dras mot varandra och bilda salter.

Elektroder
De metaller eller kolstavar som har kontakt med lösningen kallas elektroder. Elektroden som är kopplad till pluspolen kallas anod och den som är kopplad till minuspolen kallas katod. Vid en elektrolys vandrar positiva joner till katoden där de tar upp elektroner och negativa joner till anoden där de lämnar ifrån sig elektroner. Vid elektronutbytet vid de båda elektroderna sker det kemiska reaktioner.